
Arbeitsgruppe:
Myeloide Neoplasien
Leitung: PD Dr. DI Lisa Pleyer
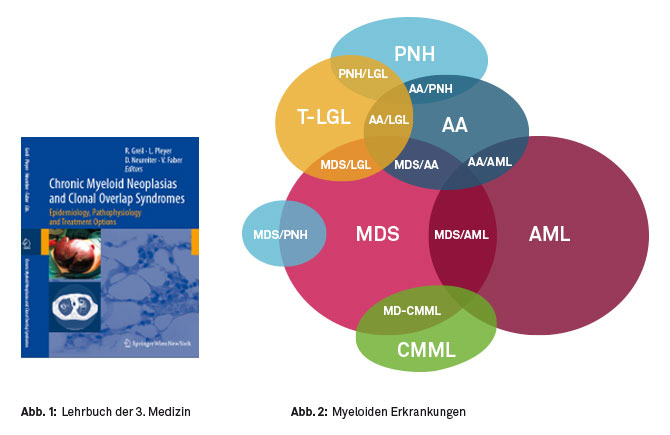
Seit 2009 beschäftigen wir uns intensiv mit Erkrankungen aus dem myloiden Formenkreis, und haben mit Assoc. Prof. Neureiter von der der hiesigen Pathologie und OÄ Dr. Viktoria Faber, die histologische bzw. zytologische Fotos zur Verfügung gestellt haben, ein Lehrbuch hierzu verfasst (Abbildung 1). Die Erkrankungen mit denen wir uns im Detail beschäftigen umfassen myelodysplastische Syndrome, akute myeloische Leukämie, chronische myelomonozytäre Leukämie, sowie diverse Übergangsformen ‚overlap syndromes‘ (Abbildung 2)
Wir haben ein nationales Datenregister gegründet, das inzwischen eines der Weltweit größten Datenregister dieser Art geworden ist, und zu vielen nationalen und internationalen Kooperationen geführt hat. Dieses Register erfasst in anonymisierter Form Daten zu Therapieverläufen, Ansprechen und Nebenwirkungen von Patienten mit diesen Erkrankungen, welche mit hypomethylierenden Substanzen behandelt wurden. Bei diesen Erkrankungen liegen sogenannte epigenetische Veränderungen vor, die einerseits Krebsgene aktivieren und andererseits auch krebsverhindernde Gene inaktivieren können. Als Resultat davon kommt es zu einer massiven Vermehrung bösartiger Stammzellen (leukämische Blasten) im Knochenmark und gleichzeitig zur Verhinderung der Ausreifung normaler Blutstammzellen zu weißen Blutkörperchen, roten Blutkörperchen und Blutplättchen.
Unter Epigenetik versteht man vererbbare Veränderungen der Genexpression und des daraus resultierenden Zellulären Phänotyps (=Erscheinungsbildes), die nicht durch Veränderungen der DNA-Sequenz zustande kommen. Ein Beispiel für die enormen Auswirkungen die epigenetische Veränderungen auf das Erscheinungsbild haben können ist z.B. die Verwandlung der raupe in einen Schmetterling (Abbildung 3). Es handelt sich dabei um dasselbe Tier, mit derselben DNA-Sequenz (=Genom). Diese ausgeprägte Veränderung des äußeren Erscheinungsbildes von der Raupe zum Schmetterling entsteht durch epigenetische Veränderungen der Genexpression (=welche Gene ‚gelesen‘ und in Proteine ‚übersetzt‘ werden). Solche epigenetischen Veränderungen sind maßgeblich an der Erkrankungsentstehung und Fortschreitung von myeloiden Neoplasien beteiligt. Hypomethylierende Substanzen können epigenetisch gesteuerten Prozess teils rückgängig machen, das Wachstum und somit Anzahl der Krebszellen verringern und fördern weiters die Ausreifung zu normalen Blutzellen.
Epigenetische Veränderungen treiben die Verwandlung von Raupe zu Schmetterling an
Die Arbeitsgruppe untersucht am weltweit größten Patientenkollektiv die Wirksamkeit verschiedener hypomethylierender Substanzen in hochunterschiedlichen Patientengruppen, und klärt die molekularen und immunologischen Mechanismen, die für den Therapieerfolg entscheidend sind. Damit sollen die Patienten mit der höchsten Wahrscheinlichkeit von gutem Ansprechen identifiziert werden. Ein weiterer Fokus liegt auf der Analyse von Chromosomen in den Krebszellen, und der Untersuchung, ob das Vorhandensein von bestimmten Mutationen ggf. das Ansprechen auf die Behandlung vorhersagen kann. Des weiteren untersucht die Gruppe die genauen Interaktionen der bösartigen Zellen mit diversen Zellen des umgebenden Immunsystems zu klären, um somit neue Ziele für zielgerichtete Therapien zu identifizieren damit noch wirksamere Behandlungskombinationen entwickelt werden können (Abbildung).
Auswirkungen der Leukämiezellen auf das Immunsystem
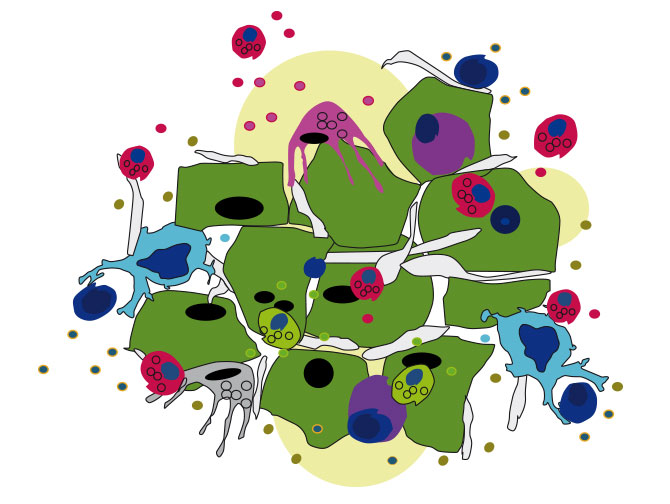
Die Krebszellen beeinflussen das Immunsystem dahingehend, dass eine Umgebung geschaffen wird, in der der Tumor ungestört wachsen kann, und die natürlichen Abwehrmechanismen des Körpers lahmgelegt werden. Diese Veränderungen kann man gezielt mittels zielgerichteter Therapien zum Teil rückgängig machen und dem Körper helfen, sich wieder effektiv gegen den Tumor zu wehren.

Ein weiterer Teil der Gruppe befasst sich mit neuen Methoden wie Blutzellen und im Blutkreislauf zirkulierende Tumorzellen voneinander effizient und sauber mittels komplexer ‚Blutfilter‘ getrennt werden können. Dies wird in Zukunft eine noch genauere Untersuchung der Tumorzellen ermöglichen.

“Wir möchten verstehen wie diese Erkrankungen die körpereigene Abwehr ‚überlisten‘, um mittels zielgerichteter Therapien gegensteuern zu können, und dem zu Körper helfen, sich wieder effektiv gegen den Tumor zu wehren.”
Team
Priv.Doz. OÄ Dr.DI Lisa Pleyer
OA Dr. Konstantin Schlick
Dr. Petra Altenhofer
(Biologin)
Dr. Thomas Barta
(Biologe)
Jakob Wagner, MSc
(Biologe)
Sie haben ein Anliegen oder Fragen?
Nehmen Sie mit uns Kontakt auf – wir melden uns umgehend bei Ihnen zurück.